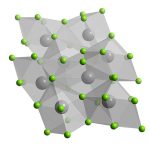
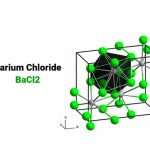
Bari clorua là dạng bột hoặc tinh thể màu trắng, dễ tan trong nước và dễ hút ẩm nên cần đậy kín và bảo quản. Khối lượng riêng tương đối của bari clorua là 3,86g / mL. Điểm nóng chảy là 963 ° C, điểm sôi là 1560 ° C, và chiết suất là 1,635. Ngọn lửa phản ứng của ion bari có màu xanh vàng.
Bari clorua thường được sử dụng làm thuốc thử phân tích, chất khử nước, muối bari, và được sử dụng trong điện tử, thiết bị đo đạc, luyện kim và các ngành công nghiệp khác.
Bari clorua là chất độc. Uống 0,2 đến 0,5 gam bari clorua có thể gây ngộ độc, và liều lượng gây chết người là khoảng 0,8 đến 1,0 gam.
Nói chung, bari clorua là dùng để chỉ bari clorua khan, vì bari clorua rất dễ hút nước, tức là nó có dạng nước tinh thể, vì vậy cần phải đậy kín và bảo quản.
Bari clorua và bari clorua khan có nhiều cách sử dụng. Các ứng dụng phổ biến bao gồm thuốc thử phân tích, chất khử nước, điều chế muối bari và điện tử, thiết bị đo đạc, luyện kim và các ngành công nghiệp khác. Nó cũng được sử dụng trong sản xuất các nguyên liệu thô muối bari khác, chẳng hạn như bari hydroxit, bari nitrat, bari cacbonat, v.v.
Ngoài ra, bari clorua còn được sử dụng rộng rãi trong sản xuất giấy, thuốc nhuộm, cao su, nhựa, gốm sứ, lọc dầu, hóa dầu, xử lý nhiệt kim loại và các gốc sunfat trong khử mặn công nghiệp clor-kiềm.
Bari clorua phản ứng với axit clohydric:
Thêm từng giọt dung dịch axit sunfuric vào dung dịch bari clorua, khi phản ứng vừa xảy ra hoàn toàn, khối lượng dung dịch không đổi, thử tìm thành phần% khối lượng của dung dịch axit sunfuric ban đầu.
Giả sử có 233g BaSO4 tạo thành kết tủa,
BaCl2 + H2SO4 = BaSO4 ↓ + 2HCl
Thêm từng giọt dung dịch axit sunfuric vào dung dịch bari clorua, đến khi phản ứng xảy ra hoàn toàn, chất lượng của dung dịch không đổi, từ phương trình: m (dung dịch axit sunfuric) = m (BaSO4),
Khi đó: m (dung dịch axit sunfuric) = 233g, m (H2SO4) = 98g,
Vậy: phần trăm khối lượng của dung dịch axit ortho-sunfuric là: 98g233g × 1 **% = 42,1%,
Phần trăm khối lượng của dung dịch axit ortho-sunfuric là 42,1%.
Muối bari là một muối vô cơ quan trọng. Kẽm bari trắng (lithopone, hỗn hợp của bari sulfat và kẽm sulfua) được sử dụng trong lớp phủ, cao su, mực in, giấy và các ngành công nghiệp khác.
Bari clorua được sử dụng trong sản xuất bột màu hữu cơ chứa bari và bari borat được sử dụng trong gốm sứ và trong công nghiệp sơn.
Bari nitrat được sử dụng để làm pháo hoa, pháo sáng, v.v. Muối bari là tên gọi chung của tất cả các muối có cation là ion bari (Ba2 +), trong đó hóa trị của bari là +2. Các muối bari thường dùng là: bari sunfat, bari nitrat, bari clorua, bari cacbonat, bari xianua, v.v.
rong quá trình sản xuất muối bari, trước hết quặng barit được khử và nung để thu được bari sulfua, sau đó bari sulfua được sử dụng làm nguyên liệu để sản xuất các muối bari khác nhau, chẳng hạn như bari sulfua phản ứng với kẽm sulfat để tạo ra kẽm bari màu trắng, phản ứng với hydro clorua để tạo ra bari clorua, phản ứng với quặng bo trong dung dịch kiềm để tạo ra bari metaborat, và phản ứng với tro soda để tạo ra bari cacbonat.
Phương trình hóa học: BaCl2 + K2SO4 → BaSO4 + 2KCl
Phương trình ion rút gọn: Ba2+ + SO42- → BaSO4 ↓