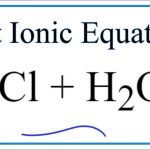Axit clohydric (axit clohidric) là dung dịch nước của hydro clorua (HCl), là một axit vô cơ đơn bazơ mạnh, được sử dụng rộng rãi trong công nghiệp. Axit clohydric là một chất lỏng không màu và trong suốt, có mùi hăng nồng và tính ăn mòn cao.
Axit clohydric đậm đặc (khoảng 37% khối lượng) rất dễ bay hơi, do đó khí hiđro clorua sẽ bay hơi sau khi mở bình chứa axit clohiđric đậm đặc và kết hợp với hơi nước trong không khí tạo ra các giọt axit clohiđric nhỏ, làm xuất hiện axit ở trên miệng chai. Axit clohydric là thành phần chính của axit dạ dày, có thể thúc đẩy quá trình tiêu hóa thức ăn và chống lại các bệnh nhiễm trùng do vi sinh vật gây ra.
Axit clohydric đậm đặc là axit clohydric có phần khối lượng của hiđro clorua vượt quá 20%. Nồng độ của axit clohydric đậm đặc bán sẵn trên thị trường là 36% ~ 38%, và nồng độ của axit clohydric đậm đặc thử nghiệm nói chung là 36% ~ 38%, là một hỗn hợp azeotropic. Axit clohydric đậm đặc rất dễ bay hơi trong không khí và nó có tính ăn mòn mạnh đối với da và quần áo.
Hydro clorua (HCl) là một hợp chất bao gồm một nguyên tử hydro và một nguyên tử clo, nguyên tử hydro và nguyên tử clo được liên kết bằng liên kết đơn cộng hóa trị có cực. Hydro clorua thường là một chất khí không màu, có thể được tạo ra bằng các phương pháp tự nhiên như núi lửa phun trào, hoặc là sản phẩm phụ của các hoạt động của con người trong quá trình đốt cháy một số loại nhựa.
Mangan đioxit là một hợp chất vô cơ có công thức hóa học là MnO2. Nó là bột vô định hình màu đen hoặc tinh thể trực thoi màu đen. Nó khó tan trong nước, axit yếu, kiềm yếu, axit nitric, axit sulfuric lạnh và hòa tan trong axit clohydric đậm đặc dưới đun nóng để tạo ra khí clo. Được sử dụng để điều chế muối mangan, và cũng được sử dụng như một chất oxy hóa, chất tẩy gỉ và chất xúc tác.
Mangan đioxit là một oxit lưỡng tính. Nó là một chất rắn dạng bột màu đen rất ổn định ở nhiệt độ phòng và có thể được sử dụng làm chất khử cực cho pin khô.
Trong phòng thí nghiệm, người ta thường dùng tính oxi hóa của nó để sản xuất khí clo bằng cách cho phản ứng với HCl đặc:
MnO2 + 4HCl = MnCl 2 + C1 2 + 2H2O
Mangan đioxit là một chất oxy hóa mạnh trong môi trường axit và kiềm. Nó phản ứng với axit sunfuric đặc để tạo ra oxy; phản ứng với axit clohydric đậm đặc để tạo ra clo. Mangan đioxit phản ứng với muối ăn da nóng chảy trong không khí tạo thành kali manganat (K2MnO4). Mangan đioxit được sử dụng làm chất tạo màu cho pin khô, thủy tinh và gốm sứ, và sản xuất mangan.
KMnO4 có thể oxi hóa HCl thành Cl2, người ta thường dùng axit clohydric đặc. Phương trình phản ứng:
2KMnO4 + 16HCl (đặc) == 2KCl + 2MnCl2 + 5Cl2 ↑ + 8H2O
Phản ứng có thể được thực hiện ở nhiệt độ phòng.
Mangan đioxit tự nhiên là pyrolusit. Nó là một chất oxy hóa mạnh và không thể bị nung nóng hoặc cọ xát với chất hữu cơ hoặc các chất khử khác như lưu huỳnh, sunfua, photphua, v.v. Mangan đioxit có thể được sử dụng làm chất màu đen hoặc tím trong men tráng men, kính thủy tinh, gốm sứ, v.v … nó có thể được sử dụng làm chất xúc tác trong ngành công nghiệp cao su; nó có thể được thêm vào sắt – kính màu để loại bỏ màu xanh lá cây; nó cũng có thể được sử dụng để tạo ra các hợp chất mangan.
MnO2 một sản phẩm công nghiệp muối vô cơ quan trọng. Tinh thể đen hoặc xám đen hoặc bột vô định hình. Nó không hòa tan trong nước và phản ứng với cacbon ở nhiệt độ cao để tạo ra mangan kim loại. Nó là một chất lưỡng tính, có hiệu suất hấp phụ tốt và khả năng oxy hóa mạnh.