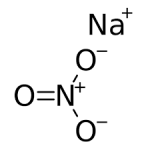
Natri nitrat là một loại muối vô cơ, công thức hóa học là NaNO3, dạng bột rắn màu trắng, còn được gọi là muối Chile hoặc muối Peru (ít phổ biến hơn). Khối lượng phân tử là 84,99. Dung dịch nước của nó là trung tính và độ pH khoảng 6,7 ~ 7,3. Mỏ natri nitrat lớn nhất trên thế giới nằm ở sa mạc Atacama ở Chile.
Tinh thể hình tam giác hút ẩm, không màu và trong suốt. Phân hủy khi đun nóng đến 380 ° C. Nó rất dễ hòa tan trong nước và amoniac lỏng, hòa tan trong metanol và etanol, rất ít hòa tan trong axeton và rất ít hòa tan trong glycerin.
Khi hòa tan trong nước, nó hấp thụ nhiệt, dung dịch trở nên lạnh và dung dịch nước là trung tính. Nó thu được bằng cách hấp thụ các oxit nitơ trong dung dịch kiềm được sử dụng trong sản xuất công nghiệp, sau đó bay hơi và kết tinh. Được sử dụng trong sản xuất axit nitric và natri nitrit, làm thành phần trong thủy tinh, diêm, men hoặc gốm công nghiệp, phân bón và chất xúc tác trong công nghiệp axit sulfuric.
Natri nitrat là một chất oxy hóa mạnh, có thể giúp ngọn lửa khi bắt lửa bằng các vật liệu dễ cháy. Khi tiếp xúc với các chất dễ oxi hóa, lưu huỳnh, chất khử và axit mạnh, nó có thể gây cháy và nổ. Khi đốt có ngọn lửa màu vàng, sinh ra khí nitơ oxit độc hại, có tác dụng kích thích da. Uống một lượng lớn có thể gây viêm dạ dày ruột, đau bụng, nôn mửa, rối loạn nhịp tim, mạch không đều và các triệu chứng khác.
Natri nitrat có thể được tổng hợp theo công thức hóa học sau:
NaOH (aq) + HNO3 (aq) → NaNO3 (aq) + H2O (l)
Natri nitrat được đun nóng đến 380 ° C để phân hủy tạo ra natri nitrit và oxy.
Natri nitrat có tính oxi hóa và có thể phản ứng với chì để tạo ra natri nitrit và oxit chì. Nó cũng oxy hóa axit hydroiodic thành iốt và tạo thành oxit nitric ở nhiệt độ phòng:
2NaNO3 + 8HI = 2NaI + 3I2 + 2NO ↑ + 4H2O
Việc đưa các ion hydro vào dung dịch natri nitrat sẽ cho thấy các đặc điểm của axit nitric:
4NaNO3 + 4H2SO4 → (đun nóng) 4NaHSO4 + 4NO2 ↑ + O2 ↑ + 2H2O
NaNO3 (aq) + 3FeCl2 + 4HCl → (đun nóng) NaCl + 3FeCl3 + NO ↑ + 2H2O
NaHSO4 + HNO3 → NaNO3 + H2SO4
Đun nóng natri nitrat và natri oxit trong chén bạc ở 700 ° C. Sau khoảng 7 ngày sẽ hình thành các tinh thể màu trắng của natri nitrat ban đầu (Na3NO4), rất nhạy cảm với hơi nước và khí cacbonic.
Natri nitrat là nguyên liệu để sản xuất kali nitrat, thuốc nổ mìn, axit picric, thuốc nhuộm, v.v. Chất nitrat hóa để sản xuất chất trung gian thuốc nhuộm. Trong ngành công nghiệp thủy tinh, nó được sử dụng như một chất khử bọt, khử màu, chất làm trong và thông lượng oxy hóa trong sản xuất các loại thủy tinh khác nhau và các sản phẩm của chúng.
Trong công nghiệp men, nó được sử dụng như một chất oxy hóa và chất trợ dung để chuẩn bị bột men. Được sử dụng như một chất làm sạch kim loại trong ngành công nghiệp máy móc và cũng được sử dụng để tạo thành một chất thổi cho kim loại đen. Được sử dụng trong công nghiệp luyện kim như một chất xử lý nhiệt để luyện thép và hợp kim nhôm. Công nghiệp nhẹ được sử dụng như một chất hỗ trợ đốt cháy cho thuốc lá.
Ngành công nghiệp dược phẩm được sử dụng làm môi trường nuôi cấy penicillin. Công nghiệp phân bón được sử dụng như một loại phân bón tác dụng nhanh thích hợp cho đất chua, đặc biệt cho các loại cây lấy củ như củ cải đường, củ cải. Nó cũng được sử dụng như một chất khử màu cho xút nóng chảy.