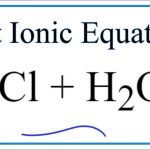Natri là một nguyên tố hóa học, ký hiệu hóa học là Na, số nguyên tử là 11, trọng lượng nguyên tử là 22,98976928 u. Nó là một kim loại màu trắng bạc mềm.
Natri là một nguyên tố ở nhóm đầu tiên của bảng tuần hoàn và là một thành viên của các kim loại kiềm. Vì lớp vỏ hóa trị của nó chỉ có một electron độc thân nên rất dễ bị mất electron để tạo thành cation Na + mang điện tích dương. Đồng vị bền duy nhất của natri là natri-23.
Natri kim loại nguyên chất không tồn tại trong tự nhiên và phải được điều chế bằng các hợp chất chứa natri. Natri là nguyên tố phong phú thứ sáu trong vỏ trái đất, và hầu hết nó tồn tại trong các khoáng chất, chẳng hạn như fenspat, sodalit và đá muối (NaCl).
Hầu hết các muối natri có tính hòa tan cao: hàng trăm triệu ion natri được hòa tan trong nước từ các khoáng chất, vì vậy ion natri và ion clorua là những nguyên tố phổ biến nhất trong số các nguyên tố hòa tan trong đại dương.
Các hợp chất của natri có nhiều ứng dụng, chẳng hạn như NaOH (dung dịch kiềm) có thể được sử dụng trong sản xuất xà phòng và NaCl (muối ăn) có thể được sử dụng làm chất khử ẩm.
Natri là một nguyên tố cần thiết cho tất cả động vật và thực vật. Ion natri là cation quan trọng nhất trong dịch ngoại bào (ECF), có ảnh hưởng quan trọng đến áp suất thẩm thấu của dịch ngoại bào và khoảng thời gian của dịch ngoại bào.
Việc mất nước trong khoảng thời gian sẽ gây ra nồng độ ion natri, tình trạng này được gọi là tăng natri máu. Sự mất đẳng trương của nước và ion natri trong ngăn chứa dịch ngoại bào làm cho kích thước của ngăn nhỏ hơn, tình trạng này được gọi là hạ natri máu.
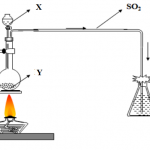
Canxi clorua được thêm vào muối nóng chảy (tức là natri clorua), đun nóng trong bể dầu và điện phân ở nhiệt độ 500 ° C và hiệu điện thế 6V. Qua quá trình điện phân, natri kim loại được tạo ra ở cực âm và clo được tạo ra ở cực dương. Sau đó, nó được tinh chế và tạo khuôn, và sau đó được đóng gói bằng parafin lỏng.
Phương trình hóa học: 2Na + Cl2 → 2NaCl
Dùng natri hydroxit làm nguyên liệu thô, cho vào thùng sắt nung chảy ở 320 ~ 330 ℃, dùng niken làm cực dương, sắt làm cực âm, đặt màng ngăn lưới niken giữa các điện cực, điện phân 4 ~ 4,5V, cực âm sẽ kết tủa natri kim loại, Và giải phóng oxy. Sau đó, natri kim loại đã chuẩn bị được tinh chế và đóng gói bằng parafin lỏng.
Phương trình hóa học: 4NaOH → 4Na + O2 + 2H2O
Trong thí nghiệm này, vì khối lượng riêng của natri nóng chảy là khoảng 0,968g / cm³ và khối lượng riêng của natri hydroxit nóng chảy là khoảng: 2,130 g / cm³, nguyên tố natri nóng chảy cuối cùng sẽ nổi ở trạng thái nóng chảy. Trên natri hydroxit, nó rất nguy hiểm khi nhanh chóng kết hợp với oxy trong không khí, vì vậy thí nghiệm này cần được thực hiện dưới sự bảo vệ của khí hiếm.
Khi cho khí tác dụng với dung dịch bromua, ta thu được hiện tượng khí màu vàng lục của clo (Cl2) mất màu dần trong dung dịch, xuất hiện khí màu da cam của brom (Br2).
Phương trình phản ứng như sau: Cl2 + 2NaBr → Br2 + 2NaCl