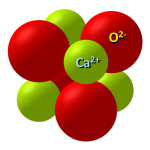
Canxi là nguyên tố kim loại có số hiệu nguyên tử là 20 và kí hiệu là Ca. Canxi là chất rắn màu trắng bạc ở nhiệt độ thường và có tính chất hóa học hoạt động, vì vậy nó chủ yếu tồn tại ở dạng ion hoặc hợp chất trong tự nhiên.
Trong một thời gian dài, các nhà hóa học coi canxi oxit thu được bằng cách nung đá vôi có chứa canxi cacbonat là một chất không thể phân chia được.
Hàm lượng canxi trong vỏ trái đất là 4,15%, chiếm vị trí thứ năm. Các khoáng chất chứa canxi chính là đá vôi CaCO3, đá dolomit CaCO3 · MgCO3, thạch cao CaSO4 · 2H2O, fluorit CaF2, apatit Ca5 (PO4) 3F, v.v.
Vỏ trứng, ngọc trai, san hô, một số vỏ động vật và đất đều chứa canxi. Clorua vôi chiếm 0,15% trong nước biển.
Canxi là kim loại hơi mềm màu trắng bạc, sáng bóng. Không tan trong benzen, ít tan trong rượu, tan trong axit và amoniac lỏng.
5Ca + 2CO2 → CaC2 + 4CaO
Nó phản ứng dữ dội với nước ở nhiệt độ phòng để tạo ra canxi hydroxit (vôi sống) và nước hydro.
Ca + 2H2O = Ca (OH) 2 + H2 ↑ (phản ứng thay thế)
Nó hòa tan trong axit và có thể phân hủy nước để giải phóng hydro. Bố cục điện tử: 1s22s22p63s23p64s2
Phương trình hóa học liên quan của canxi:
Ca + 2HCl = CaCl2 + H2 ↑ (phản ứng thay thế)
N2 + 3Ca = Ca3N2 (phản ứng kết hợp)
3C + CaO = CaC2 + CO ↑ (Phản ứng oxi hóa khử)
CaO + H2O ⟶ Ca(OH)2
CO2 + Ca (OH) 2 (dư) = CaCO3 ↓ + H2O (phản ứng phản ứng tổng hợp)
2CO2 (dư) + Ca (OH) 2 = Ca (HCO3) 2 (phản ứng cộng hợp)
SO2 + Ca (OH) 2 = CaSO3 ↓ + H2O (phản ứng phản ứng tổng hợp)
SO3 + Ca (OH) 2 = CaSO4 + H2O (phản ứng phản ứng tổng hợp)
2HNO3 + CaCO3 = Ca (NO3) 2 + H2O + CO2 ↑ (phản ứng phản ứng tổng hợp)
2Cl2 + 2Ca (OH) 2 = CaCl2 + Ca (ClO) 2 + 2H2O (phản ứng oxi hóa khử)
CaH2 + 2H2O = Ca (OH) 2 + 2H2 ↑ (phản ứng oxi hóa khử)
2HF + CaCl2 = CaF2 + 2HCl (phản ứng phản ứng tổng hợp)
SiO2 + CaO = CaSiO3 (phản ứng kết hợp)
CaCO3 = CaO + CO2↑ (Phản ứng phân hủy)
Ca(HCO3)2= CaO + H2O + CO2↑(Phản ứng phân hủy)
Đầu tiên, canxi clorua thu được bằng phản ứng giữa đá vôi và axit clohiđric:
CaCO3 + 2HCl = CaCl2 + H2O + CO2 ↑
Trong phương pháp điện phân, người ta cho canxi clorua khan đã sấy khô vào bình điện phân, phun nguyên liệu bên cạnh anot (than chì) trong bình điện phân với ngọn lửa oxyaxetilen, tức là đun sôi nước để nguội, đặt catot xuống.
Dòng điện được truyền tới bề mặt chất lỏng. Vật liệu nóng chảy chảy tới cực âm để nối mạch. Sau khi phần lớn nguyên liệu đã nấu chảy, tiếp tục cho nguyên liệu mới vào cho đến khi cách mép rãnh từ 2 đến 3 cm và nhiệt độ bình thường.
Kim loại canxi cho vào catôt dòng điện 350-450 A và hiệu điện thế 20-25 V. Trước khi cho kim loại canxi lắng vào catôt thì dòng điện phải giảm 50-100A.
Sau khi cho can xi kim loại bị gõ vào dầu, catôt lại tiếp xúc với bề mặt bình điện phân thì thấy cường độ dòng điện tăng thêm 50-100 A. Để duy trì nhiệt độ của bình điện phân, cần tiếp tục nạp liệu. Khí clo thoát ra từ anot và được tái chế.
CaCl2 → Ca + Cl2↑ (Lấy canxi và clo phụ phẩm)
Có thể thu được canxi bằng phương pháp điện phân và nhiệt phân. Độ tinh khiết của muối canxi clorua nóng chảy sau điện phân chỉ đạt 90%. Phương pháp khử nhiệt sử dụng nhôm để khử canxi oxit ở nhiệt độ cao, và độ tinh khiết của sản phẩm cao (99%).
Đầu tiên, CaO được tạo ra bằng cách nung CaCO3. Tốt nhất là nhôm có dạng hạt nhỏ hoặc mảnh. Tỉ lệ số mol của canxi oxit đối với nhôm là 3: 2. Sau khi các thành phần được trộn đều, một mẫu trắng sẽ được tạo ra. Áp suất của máy ép thủy lực bằng tay có thể thấp hơn áp suất của phôi magie-silicon.